替國產疫苗背書 陳時中:擴大規模、安全性不會有問題
 ▲針對國產疫苗沒有進入三期試驗,已發各界熱議。示意圖(圖/NOWnews資料照片)
▲針對國產疫苗沒有進入三期試驗,已發各界熱議。示意圖(圖/NOWnews資料照片)
記者劉雅文/綜合報導
中央流行疫情指揮中心今(31)日公布國內新增278例COVID-19確定病例,分別為274例本土個案及4例境外移入個案;另有校正回歸本土個案73例,總計351例。確診個案中新增15例死亡。
針對國產疫苗爭議,指揮官陳時中表示,以國產疫苗一、二期受試人數跟國際比較,算是擴大的試驗,陳提到,國產疫苗做了將近4000人,以這樣的規模比國外一、二期數目大很多,可以視為二、三期延續計畫,以這樣規模如果能夠通過,安全性就不會有問題。
 ▲各場疫苗受試人數比較一覽表。(圖/指揮中心提供)
▲各場疫苗受試人數比較一覽表。(圖/指揮中心提供)
陳時中舉例,以國外疫苗為例,BNT新冠疫苗三期結果出來,其實也是要到2023年4月,另外莫德納的三期結果則是到2022年10月,嬌生也是在2023年5月。陳時中強調,雖然三期都還沒完成,可是各國都已經通過EUA緊急授權使用,等到三期試驗完畢,恐怕緩不濟急。
另外有媒體提到,有檢察官提出應該要公布購買疫苗價格,對此,陳時中回應,檢察官需要了解可以訊問,但指揮中心是關心臨床試驗有沒有照規格,以及相關解盲結果,來做為我們EUA參考。
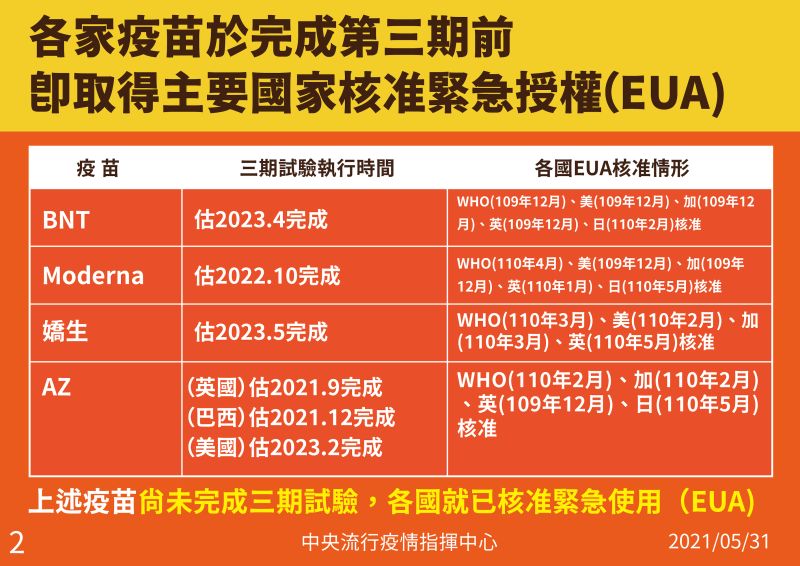 ▲各場疫苗完成緊急授權日期。(圖/指揮中心提供)對於國產疫苗的爭議,林氏璧指出,目前國外大廠疫苗如輝瑞BNT、莫德納、AZ與嬌生,皆經過初步的3期試驗之後,確認至少有50%以上保護力,才取得EUA,目前僅有中國、俄羅斯是疫苗做完2期試驗就直接取得EUA,「我們的第2期有故意增加人數到3000人,但這樣能不能取代第3期?我想這裡就很見仁見智了。」
▲各場疫苗完成緊急授權日期。(圖/指揮中心提供)對於國產疫苗的爭議,林氏璧指出,目前國外大廠疫苗如輝瑞BNT、莫德納、AZ與嬌生,皆經過初步的3期試驗之後,確認至少有50%以上保護力,才取得EUA,目前僅有中國、俄羅斯是疫苗做完2期試驗就直接取得EUA,「我們的第2期有故意增加人數到3000人,但這樣能不能取代第3期?我想這裡就很見仁見智了。」
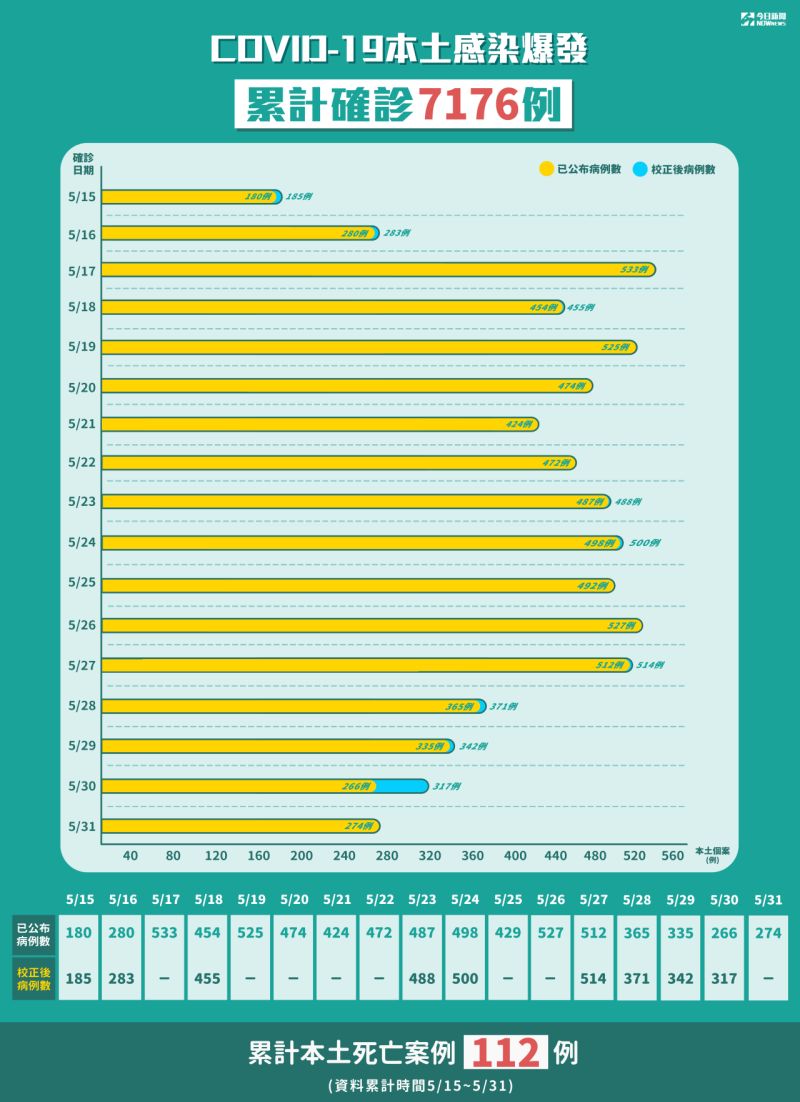 ▲指揮中心今(31)日公布新增274例本土個案,另有73例校正回歸個案,5/15至今累計7176例本土確診、112個死亡案例。(圖/NOWnews製作)
▲指揮中心今(31)日公布新增274例本土個案,另有73例校正回歸個案,5/15至今累計7176例本土確診、112個死亡案例。(圖/NOWnews製作)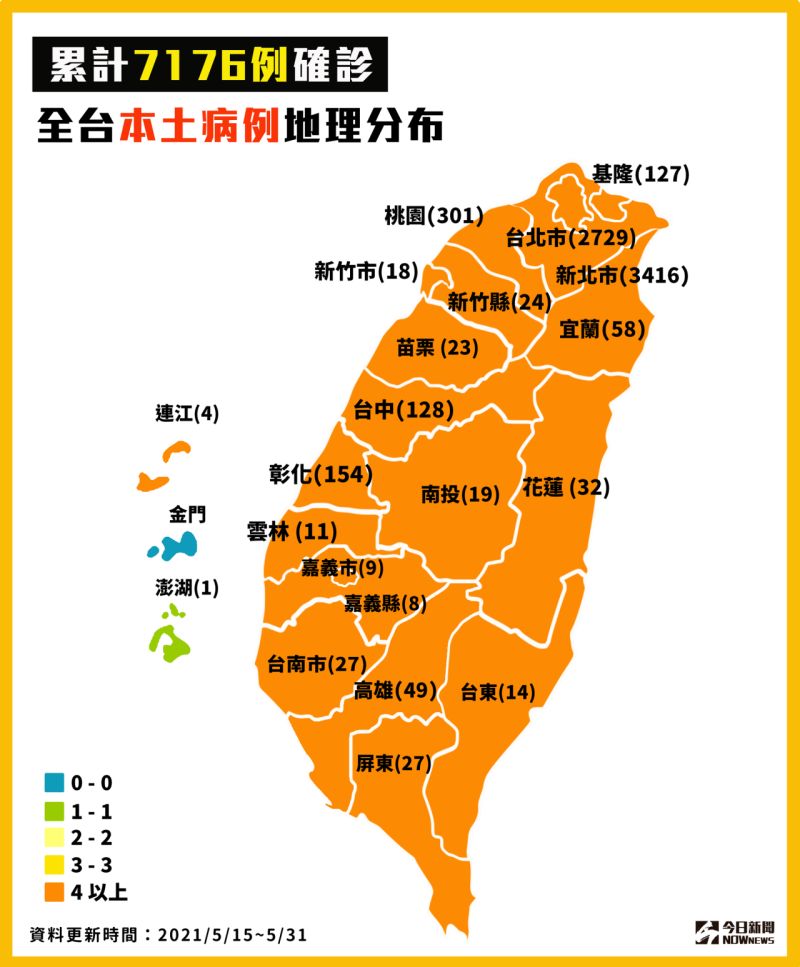 ▲指揮中心今(31)日公布新增274例本土個案,外島地區除了連江縣之外,澎湖縣也淪陷。(圖/NOWnews製作)
▲指揮中心今(31)日公布新增274例本土個案,外島地區除了連江縣之外,澎湖縣也淪陷。(圖/NOWnews製作)
※【NOWnews 今日新聞】提醒您:
因應新冠肺炎疫情,疾管署持續加強疫情監測與邊境管制措施,國外入境後如有發燒、咳嗽等不適症狀,請撥打「1922」專線,或「0800-001922」,並依指示配戴口罩儘速就醫,同時主動告知醫師旅遊史及接觸史,以利及時診斷及通報。







